この反応における観察できる反応は,
では,逐次反応の場合の持続時間の分布を計算してみましょう.
![]()
この反応における観察できる反応は,
と単純化できます.
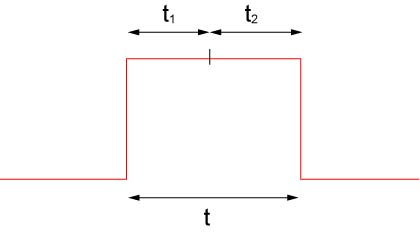
我々が観察している持続時間は,t,です.
二つの反応,それぞれのイベントは判定することができません.
もし,最初のイベントが,t1,であったなら,その次のイベントは,t2=t-t1,とならなければなりません.
t1,t2,おのおのの時間である確率は,それぞれの時定数,α,βによって決まり,
![]()
となります.
規格化をすると,各反応の分布は,
![]()
となります.
つまり,t,であるためには,それぞれの確率の積となりますね.
そして,その,t1,を0~t,に渡って積分すればいいのですから,
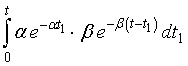
が求めたい,t,の分布となります.
解は,
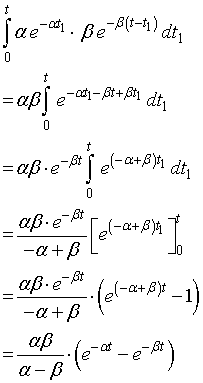
ここで,係数はヒストグラムには関係ありませんので,
![]()
となります.
二つの指数関数の差,ですね.
この分布の様子は,
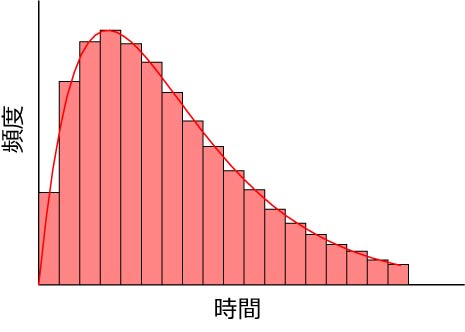
となります.
2003年の論文,
Kimura, Y., Toyoshima, N., Hirakawa, N., Okamoto, K. & Ishijima, A. (2003). A kinetic mechanism for the fast movement of Chara myosin. Journal of Molecular Biology 328, 939-950.
のFig.5を見ていただけるとわかりやすいのですが,
1 uM : 11.2, 10.5 s-1
10 uM : 1025 s-1
1 mM : 10.4 s-1
となっています.
低ATP濃度では,上記の考えのように,二つの指数関数の差で表せたのに,ATP濃度が高くなると,一つ指数関数となります.
これは,
新しいATPの結合
のレートがATP濃度により,ATP濃度が上がるほど速くなるからです.
このレートが速くなり,我々の実験系では無視できる程度になり,結局として,ADPの解離のみの反応のように,見えるためです.
このような解析を用いることにより,1分子の力学計測でありながら,化学反応も併せて見いだすことができるのです.
では,もう一つステップが増えた場合はどうなるのでしょう?